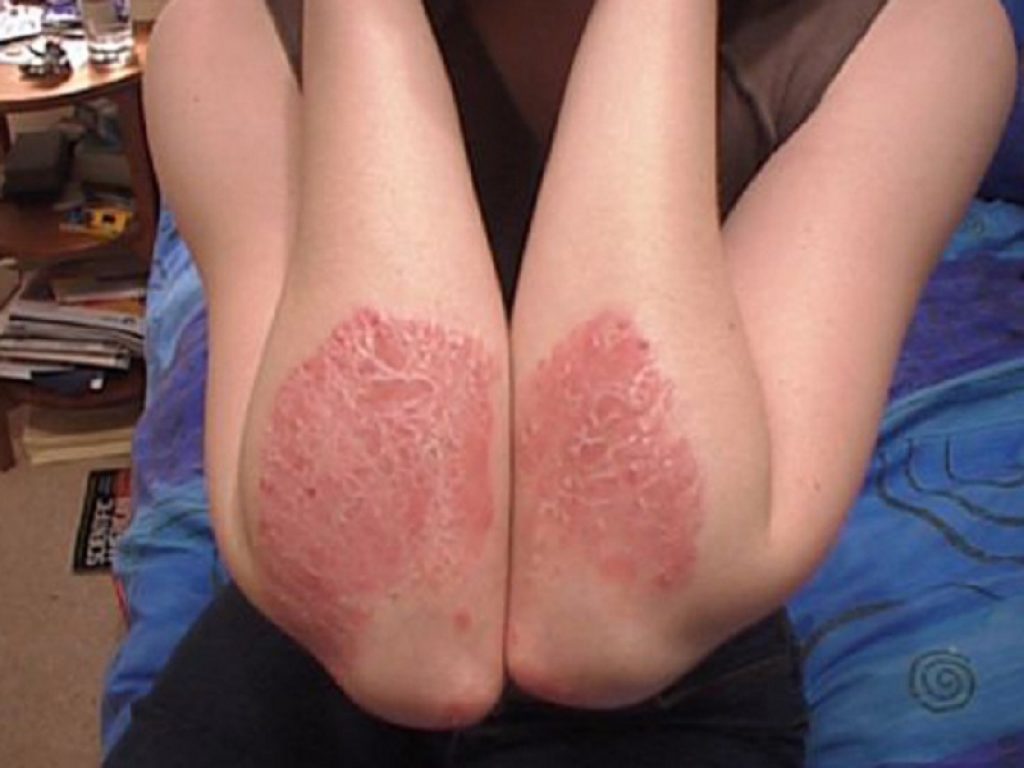
Psoriasi a placche: miglioramenti nei pazienti con l’agente sperimentale tapinarof in crema ma con diversi effetti collaterali
Una crema contenente il farmaco sperimentale tapinarof ha migliorato significativamente la psoriasi a placche in circa un terzo dei pazienti, ma ha sovente provocato diversi effetti collaterali come cefalea, follicolite e dermatite da contatto, secondo i risultati di due studi di fase III pubblicati di recente sul New England Journal of Medicine.
L’agente modulante del recettore degli idrocarburi arilici da somministrarsi una volta al giorno è attualmente in fase di valutazione da parte della Food and Drug Administration e una decisione è prevista nel secondo trimestre del 2022. Tapinarof modula l’espressione dell’interleuchina-17 e delle proteine di barriera cutanea filaggrina e loricrina.
«Tapinarof fa parte di una nuova classe di molecole che hanno un meccanismo d’azione mai usato prima, ma l’importante è che non sia uno steroide» ha affermato il primo autore Mark Lebwohl, presidente del Kimberly ed Eric Waldman Department of Dermatology presso la Icahn School of Medicine del Mount Sinai. «Quando trattiamo la psoriasi, i farmaci più comunemente prescritti sono gli steroidi e hanno molti effetti collaterali. Un’opzione di trattamento non steroidea potrebbe evitarli, in particolare l’atrofia della pelle, che è un problema comune in aree come l’inguine, le ascelle e il viso».
Due studi di fase III
I due studi di fase III PSOARING-1 e PSOARING-2 con un disegno identico hanno valutato tapinarof in crema all’1% una volta al giorno rispetto al solo veicolo. I pazienti arruolati, rispettivamente 510 e 515, erano volontari adulti con psoriasi da lieve a grave e con una percentuale di cute interessata dalla malattia compresa tra il 3 e il 20%.
L’endpoint primario di efficacia era il raggiungimento di un punteggio di 0/1 (pelle libera o quasi libera da lesioni) nel Physician Global Assessment (PGA), con una diminuzione di almeno 2 punti rispetto al basale dopo 12 settimane.
Gli endpoint secondari includevano una diminuzione di almeno il 75% dello Psoriasis Area and Severity Index (PASI 75), il raggiungimento del PASI 90 e la variazione media della percentuale della superficie corporea totale (BSA) interessata. Gli esiti riportati dai pazienti includevano una riduzione della Peak Pruritus Numeric Rating Scale (PP-NRS), un cambiamento nel Dermatology Life Quality Index (DLQI) e la variazione media dei punteggi dello Psoriasis Symptom Diary.
Buone risposte di efficacia
Alla settimana 12 la risposta PGA è stata raggiunta dal 35,4% del gruppo tapinarof rispetto al 6% del gruppo veicolo in PSOARING 1 e dal 40,2% del gruppo di trattamento rispetto al 6,3% del gruppo veicolo in PSOARING 2.
Una risposta PASI 75 è stata registrata rispettivamente nel 36,1% e nel 47,6% dei soggetti trattati, rispetto al 10,2% e al 6,9% di quelli sottoposti a veicolo, mentre la risposta PASI 90 è stata osservata nel 18,8% e nel 20,9% nei due gruppi di trattamento, rispetto all’1,6% e al 2,5% nei rispettivi gruppi veicolo.
Inoltre, il coinvolgimento della BSA ha mostrato una diminuzione media di -3,5 punti percentuali dopo 12 settimane nel gruppo tapinarof del primo trial rispetto a -0,2 nel gruppo del veicolo. Nel secondo studio la riduzione della BSA è stata simile, con una diminuzione media del 4,2% nel gruppo tapinarof e dello 0,1% con il solo veicolo.
Il prurito, misurato dal punteggio PP-NRS riportato dal paziente, è stato ridotto in media di 3,6 e 3 punti nei gruppi di trattamento, rispetto a 2,7 e 1,4 punti nei controlli. Una diminuzione di almeno 4 punti nel PP-NRS è stata riportata dal 60,7% e dal 56,9% dei soggetti trattati che avevano un punteggio basale di almeno 4, contro il 43,2% e il 29,6% dei controlli.
I punteggi DLQI hanno avuto una variazione media di -4,6 nel gruppo tapinarof e di -2,8 nel gruppo veicolo nel primo studio e di -4,4 nel gruppo di trattamento e di -1,1 nei controlli nel secondo studio.
A fine settembre 2021 la compagnia sviluppatrice (Dermavant Sciences) ha pubblicato i risultati del trial di estensione in aperto PSOARING 3, nel quale dopo ulteriori 40 settimane di trattamento, il 58% dei 519 volontari che hanno iniziato con un punteggio PGA di 2 o superiore ha ottenuto un punteggio di 0 o 1, dimostrando il continuo miglioramento dell’efficacia del farmaco oltre la durata dei primi due studi.
Diversi effetti collaterali
Dei 683 pazienti assegnati in modo casuale a ricevere tapinarof nei due studi il 20,1% ha sviluppato una follicolite, che ha portato all’interruzione del trattamento nell’1,3% dei casi. Con la crema veicolo il tasso di follicolite è stato dello 0,9%.
La dermatite da contatto si è verificata nel 5,4% dei soggetti in trattamento attivo rispetto a un solo paziente nel gruppo di controllo e nell’1,8% dei casi ha portato all’interruzione della terapia.
La cefalea si è verificata nel 3,8% del gruppo tapinarof rispetto all’1,5% nel gruppo di controllo e ha comportato l’interruzione del trattamento in tre pazienti.
Bibliografia
Lebwohl MG et al. Phase 3 Trials of Tapinarof Cream for Plaque Psoriasis. N Engl J Med. 2021 Dec 9;385(24):2219-2229.
Leggi