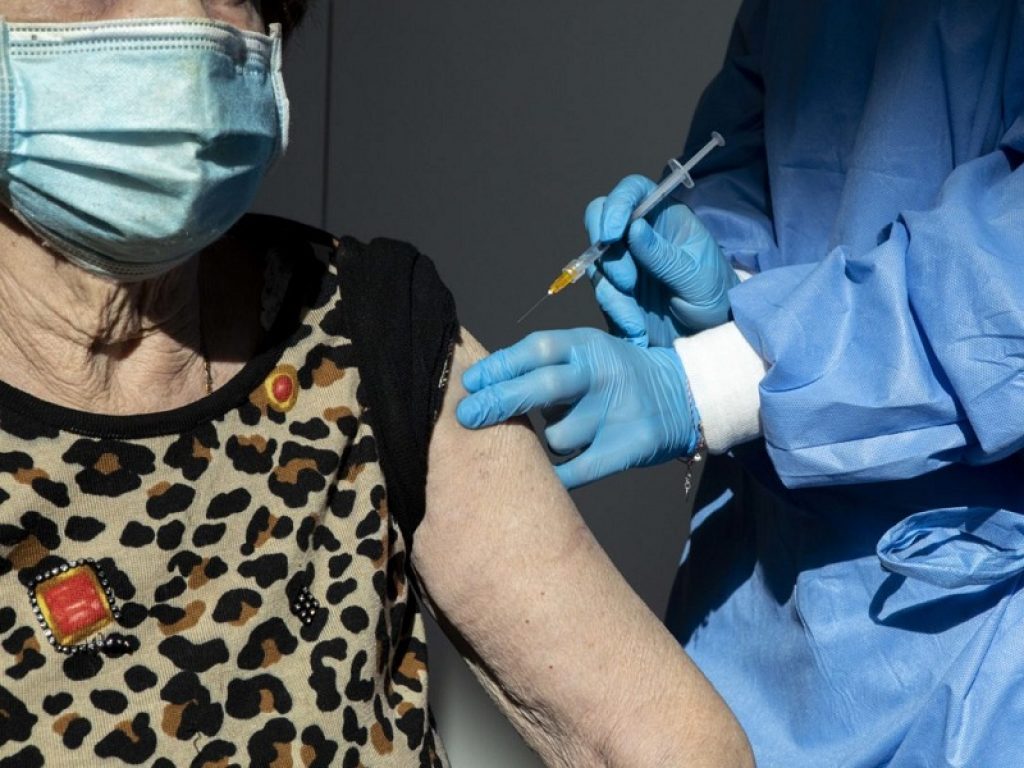
Vaccini anti-Covid: per gli immunodepressi “serve strategia personalizzata”. I risultati di 5 studi su diverse tipologie di soggetti fragili di età compresa tra i 12 e i 25 anni
Il ricorso ai vaccini contro il SARS-CoV-2 per i pazienti immunodepressi è fondamentale, ma nei soggetti particolarmente fragili la loro efficacia può essere minore a causa della patologia di base e o delle terapie a cui sono sottoposti. È quanto è emerso da un gruppo di 5 studi, denominato CONVERS, condotti dai ricercatori del Bambino Gesù su diverse tipologie di pazienti fragili compresi tra i 12 e i 25 anni. L’ultimo studio, su bambini e ragazzi affetti da infezione perinatale da HIV, è stato appena pubblicato sulla rivista Clinical Infectious Diseases.
«La maggior parte dei soggetti immunodepressi – spiega Paolo Palma, responsabile di Immunologia Clinica e Vaccinologia dell’Ospedale della Santa Sede – risponde al vaccino ma in misura minore rispetto ai soggetti sani, con delle differenze da gruppo a gruppo, mentre una percentuale minoritaria non sviluppa purtroppo alcuna forma di immunità al virus. Per questi pazienti fragili è importante intervenire con una strategia vaccinale di rinforzo e personalizzata».
I 5 STUDI “CONVERS”
Gli studi sull’efficacia dei vaccini anti-COVID sugli immunodepressi sono stati condotti dai ricercatori dall’Unità di ricerca di Immunologia Clinica e Vaccinologia su 5 diverse categorie di bambini e ragazzi: con immunodeficienza primitiva, trapiantati di cuore/polmone, con malattia infiammatoria cronica intestinale, con Sindrome di Down e con infezione perinatale da HIV.
Le indagini fanno parte del progetto denominato CONVERS, e sono state pubblicate, rispettivamente, sulle riviste scientifiche Frontiers in Immunology, Transplantation, Vaccines, Journal Clinical Medicine e Clinical Infectious Diseases. I primi due studi, quelli su immunodeficienza primitiva e trapianti di cuore/polmone erano stati pubblicati a ottobre 2021.
I progetti di ricerca sono stati condotti su una coorte complessiva di 165 pazienti di età compresa tra i 12 e i 25 anni, di cui 21 affetti da immunodeficienza primitiva, 34 sottoposti a trapianto di cuore e polmone (30 cuore, 2 cuore-rene, 2 polmone), 30 da malattia infiammatoria cronica intestinale, 40 da Sindrome di Down e 40 da HIV.
Nei vari gruppi è stata analizzata la risposta alle prime due dosi del vaccino Pfizer, sia quella sierologica (cioè la quantità di anticorpi presenti nel sangue) che, in 3 dei 5 gruppi, quella cellulare (ovvero la presenza di linfociti T specifici contro il SARS-CoV-2 e, nel caso dei trapiantati di fegato e rene, dei linfociti B). I dati sono stati poi confrontati con quelli di gruppi di controllo composti da persone sane, sottoposte alla vaccinazione anti-COVID nello stesso periodo.
I RISULTATI
Dai 5 studi emerge che la maggior parte dei bambini immunodepressi risponde al vaccino – risultato confortante – anche se in misura generalmente minore rispetto ai soggetti sani (meno anticorpi e meno linfociti specifici contro il SARS-CoV-2) e con delle differenze da gruppo a gruppo, mentre una percentuale minoritaria di soggetti – particolarmente immunocompromessi – non sviluppa alcuna forma di immunità al virus.
Nel dettaglio, per quanto riguarda l’indagine sui pazienti con infezione perinatale da HIV (condotta in collaborazione col Dipartimento Pediatrico Universitario Ospedaliero del Bambino Gesù), l’analisi sierologica ha rilevato che il 100% dei ragazzi ha sviluppato anticorpi specifici per SARS-COV-2, ma significativamente inferiori rispetto al dato medio del gruppo di controllo. L’analisi cellulare ha invece rilevato nell’89% dei casi una mancata di espansione di linfociti T specifici a causa della condizione infiammatoria di base tipica dell’HIV e della capacità da parte del sistema immunitario del paziente di controllarla.
Nella ricerca sui soggetti con malattia infiammatoria cronica, condotta in collaborazione col Dipartimento di Pediatrie Specialistiche e Trapianto Fegato Rene, l’analisi sierologica ha mostrato una buona risposta, comparabile al gruppo di controllo. Tuttavia nei pazienti che utilizzano farmaci anti-TNF, degli anticorpi monoclonali per il trattamento di questa patologia, la risposta sierologica si è rivelata inferiore in media del 43% rispetto al gruppo con regimi terapeutici immunosoppressivi senza anti-TNF. In questi pazienti la causa della minore efficacia dipende quindi dalla tipologia di trattamento che seguono.
Lo studio sulla coorte con Sindrome di Down è stato realizzato con la collaborazione del Dipartimento di Emergenza, Accettazione e Pediatria Generale e ha rivelato in tutti i pazienti una risposta sierologica, ma comparabile a quella degli adulti di età superiore ai 65 anni. Quindi molto inferiore rispetto ai pari età sani. Il problema della minore risposta risiede nell’invecchiamento precoce del sistema immunitario tipica di questa sindrome.
Per quanto riguarda l’indagine sui pazienti con immunodeficienza primitiva, l’analisi sierologica ha rilevato che il 14% dei ragazzi non ha sviluppato anticorpi. Sul restante 86% è stata riscontrata una buona risposta anticorpale, benché inferiore al dato medio del gruppo di controllo. L’analisi cellulare ha invece rilevato l’assenza dei linfociti T specifici nel 24% dei soggetti. Le ragioni della minore efficacia in questi soggetti sono da ricercare nel malfunzionamento del sistema immunitario tipico di questa patologia. La ricerca è stata condotta in collaborazione col Dipartimento Pediatrico Universitario Ospedaliero.
Infine, lo studio sui bambini sottoposti a trapianto di cuore e polmone ha rivelato come il 31% non abbia sviluppato anticorpi. Sul restante 69% è stata registrata una risposta anticorpale, ma a livelli significativamente inferiori a quelli del gruppo di controllo. Anche sul fronte dell’analisi cellulare, l’indagine realizzata in collaborazione col Dipartimento di Cardiochirurgia, Cardiologia e Trapianto Cuore Polmone, ha evidenziato un mancato incremento di linfociti T SARS-CoV2 specifici nel 31% dei pazienti. Nei soggetti con trapianto di cuore e polmone la bassa risposta dipende dalla tipologia di trattamento a cui vengono sottoposti (quelli trattati con micofenolato hanno meno probabilità di rispondere adeguatamente).
Tutti e 5 gli studi si sono avvalsi della collaborazione del Dipartimento di Medicina Diagnostica e di Laboratorio e hanno confermato la sicurezza dei vaccini anti-SARS-CoV-2 anche per quanto riguarda i pazienti fragili: dopo la somministrazione delle dosi sono stati registrati solo effetti collaterali transitori e di lieve entità.
LE PROSPETTIVE FUTURE
Adesso si dovranno effettuare ulteriori studi per comprendere a fondo i meccanismi biologici responsabili della minore risposta vaccinale. Questo permetterà di intervenire in maniera personalizzata per ogni gruppo di bambini fragili risolvendo il problema della scarsa risposta vaccinale.
«La strategia vaccinale va adattata alle specificità di ogni gruppo di pazienti – spiega il professor Paolo Palma, responsabile di Immunologia Clinica e Vaccinologia del Bambino Gesù – Alcuni gruppi rispondono meglio a una vaccinazione eterologa, altri hanno bisogno di una formulazione specifica, altri ancora devono rimodulare i trattamenti a cui sono sottoposti e che influiscono negativamente sull’efficacia della vaccinazione. In attesa di individuare le migliori strategie vaccinale restano fondamentali le dosi aggiuntive che garantiscono comunque una valida forma di protezione in queste categorie di pazienti. La minore efficacia degli attuali vaccini anti-SARS-CoV-2 nelle diverse tipologie di soggetti fragili conferma inoltre l’importanza della vaccinazione sia dei loro caregivers che della popolazione in generale».
Proprio di vaccinazione nei pazienti fragili si occuperà la quarta conferenza internazionale sulla vaccinazione di precisione (IPVC) che si terrà dal 5 al 7 ottobre 2023 a Roma, per la prima volta in Italia, e che sarà ospitata dal Bambino Gesù in collaborazione con l’Università di Harvard e il Boston Children’s Hospital.